Gure produktu nagusiak: amino silikona, bloke silikona, silikona hidrofilikoa, silikona emultsio guztiak, bustitzeko igurtziaren iraunkortasunaren hobetzailea, uraren aurkakoa (fluorrik gabe, Karbono 6, Karbono 8), demin garbiketa produktu kimikoak (ABS, entzima, Spandex babeslea, manganeso kentzailea), xehetasun gehiago lortzeko, jarri harremanetan: Mandy +86 19856618619 (Whatsapp)
Gainazal-aktiboen sarrera
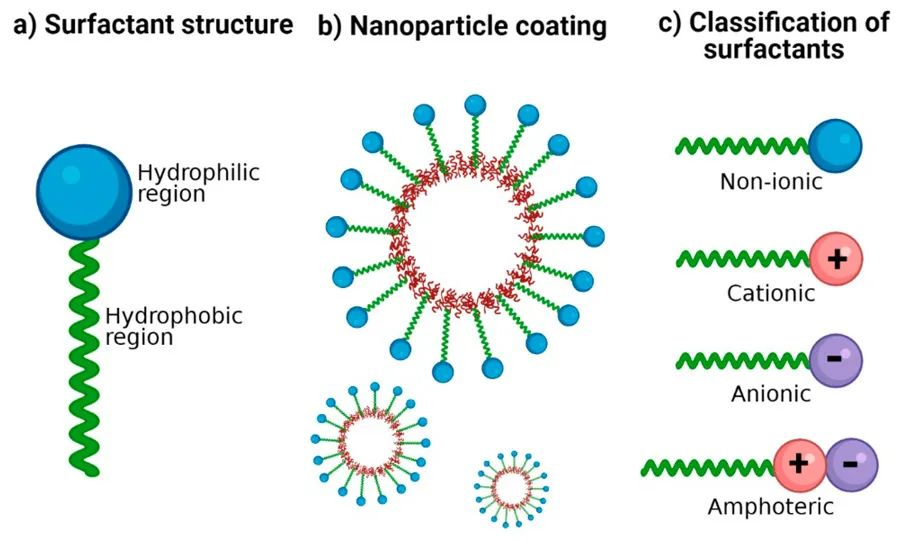
Gainazal-aktiboek egitura molekular anfifilikoa dute: mutur batek talde hidrofiliko bat dauka, buru hidrofilikoa deritzona, eta beste muturrak, berriz, talde hidrofobiko bat, isats hidrofobiko izenekoa. Buru hidrofilikoak gainazal-aktiboei monomero forman uretan disolbatzea ahalbidetzen die.
Talde hidrofilikoa askotan talde polar bat izaten da, eta karboxilo talde bat (-COOH), azido sulfoniko talde bat (-SO3H), amino talde bat (-NH2), aminak eta haien gatzak, hidroxilo taldeak (-OH), amida taldeak edo eter loturak (-O-) izan daitezke, talde hidrofilo polarretako beste adibide batzuk bezala.
Talde hidrofoboa normalean hidrokarburo-kate ez-polar bat da, hala nola alkilo-kate hidrofoboak (R- alkiloarentzat) edo talde aromatikoak (Ar- arilarentzat).
Gainazal-aktiboen sailkapena honako hauetan egin daiteke: gainazal-aktibo ionikoak (gainazal-aktibo kationikoak eta anionikoak barne), gainazal-aktibo ez-ionikoak, gainazal-aktibo anfoteroak, gainazal-aktibo mistoak eta beste batzuk. Gainazal-aktiboen disoluzioetan, gainazal-aktiboen kontzentrazioa balio jakin batera iristen denean, gainazal-aktiboen molekulek mizela izeneko hainbat agregatu ordenatu eratzen dituzte. Mizelizazio-prozesua, edo mizelen eraketa, gainazal-aktiboen disoluzioen oinarrizko propietate erabakigarria da, gainazaleko fenomeno garrantzitsu asko lotuta baitaude mizelen eraketarekin.
Gainazal-aktiboek mizelak disoluzioan sortzen dituzten kontzentrazioari Mizelen Kontzentrazio Kritikoa (CMC) deritzo. Mizelak ez dira egitura finko eta esferikoak; aitzitik, irregulartasun handia eta forma-aldaketa dinamikoak erakusten dituzte. Baldintza jakin batzuetan, gainazal-aktiboek alderantzizko mizelen egoerak ere erakuts ditzakete.
CMC-an eragina duten faktoreak:
- Gainazal-aktiboen egitura
- Gehigarrien mota eta presentzia
- Tenperatura
Gainazal-aktiboen eta proteinen arteko elkarrekintzak
Proteinek talde ez-polarrak, polarrak eta kargatuak dituzte, eta molekula anfifiliko askok modu askotan elkarreragin dezakete proteinekin. Baldintzen arabera, gainazal-aktiboek egitura desberdineko agregatu molekular antolatuak sor ditzakete, hala nola mizelak edo alderantzizko mizelak, eta hauek modu ezberdinean elkarreragiten dute proteinekin.
Proteinen eta gainazal-aktiboen (Proteina-Gainazal-aktibo, PS) arteko elkarrekintzek batez ere elkarrekintza elektrostatikoak eta elkarrekintza hidrofoboak dakartzate. Gainazal-aktibo ionikoek proteinekin elkarreragiten dute batez ere talde polarraren indar elektrostatikoen eta karbono-kate alifatikoaren elkarrekintza hidrofoboen bidez, proteinaren eskualde polarrei eta hidrofoboei lotuz, eta horrela PS konplexuak eratuz.
Gainazal-aktibo ez-ionikoek batez ere proteinekin elkarreragiten dute indar hidrofoboen bidez, non kate hidrofoboek proteinen eskualde hidrofoboekin elkarreragiten duten. Elkarrekintzak surfaktantearen eta proteinen egituran eta funtzioan eragina izan dezake. Beraz, surfaktanteen motak eta kontzentrazioak, ingurumen-testuinguruarekin batera, zehazten dute surfaktanteek proteinak egonkortzen edo desestabilizatzen dituzten, baita agregazioa edo sakabanaketa sustatzen duten ere.
Gainazal-aktiboen HLB balioa
Gainazal-aktibo batek bere gainazaleko jarduera berezia erakusteko, osagai hidrofoboak eta hidrofiloak orekatu behar ditu. HLB (Hidrofilo-Lipofilo Balantzea) gainazal-aktiboen hidrofilo-lipofilo orekaren neurria da eta gainazal-aktiboen propietate hidrofiliko eta hidrofoboen adierazle gisa balio du.
HLB balioa balio erlatiboa da (0tik 40ra bitartekoa). Adibidez, parafinak 0 HLB balioa du (osagai hidrofilikorik gabe), polietilen glikolak 20 HLB balioa du, eta SDS oso hidrofilikoak (sodio dodezil sulfatoa) 40 HLB balioa du. HLB balioa erreferentzia gisa balio dezake gainazal-aktiboen hautaketak egiterakoan. HLB balio handiago batek hidrofilikotasun hobea adierazten du, eta HLB balio baxuago batek hidrofilikotasun okerragoa.
Argitaratze data: 2024ko irailaren 10a

